DIC病因的快速判断

患者男,54岁。因“头昏半月,胸闷、呼吸困难3天”就诊,外院查肌钙蛋白升高(892pg/mL),心脏彩超未见异常,胸部CT考虑肺水肿。入我院当天血常规检查示Hb46g/L,PLT计数16*10^9/L,网织红3%,白细胞计数正常。
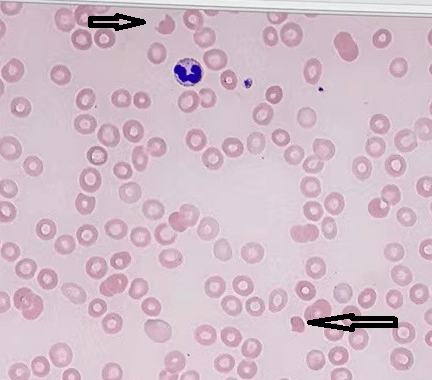
外周血涂片可见裂红细胞略增多(>1%):
凝血检查:
PT
16.8
秒(Ref 11.5-14.5)
APTT 36.6秒(Ref 29-42)
FIB:3.97g/L(Ref 2.00-4.00)
D-Dimer:
>21.0
ug/mL(Ref<0.5)
患者ISTH-DIC评分已达6分,再结合裂红细胞增多,
DIC可能性大
。微血栓形成也可以解释患者存在心肌缺血症状但无明确影像学证据。
进一步ADAMTS13活性测定:98%(Ref 65-135)结果正常,排除TTP。
肝肾功能轻度异常,也不提示HUS。
那么患者DIC的病因为何?
首先从D-dimer显著升高(超出检测上限)的可能病因分布(同济急诊数据)来看:
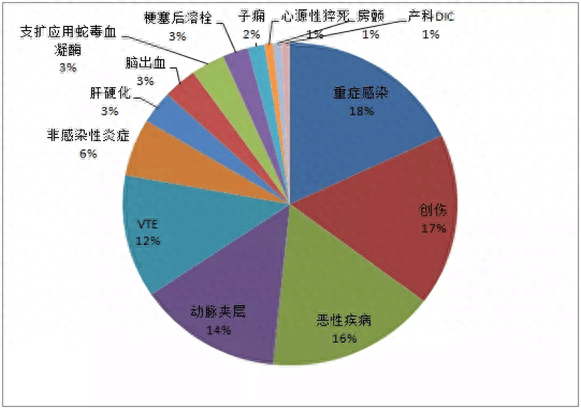
患者目前的影像学检查不提示VTE、主动脉夹层,也排除了创伤,可能性较大的病因有两个:感染和恶性疾病。
其次根据纤溶状况给DIC分型,DIC可以大致分为纤溶抑制型、均衡型和增强型,分别典型疾病为脓毒症(抑制型)、实体肿瘤(均衡型)和早幼粒细胞白血病、主动脉瘤(增强型):
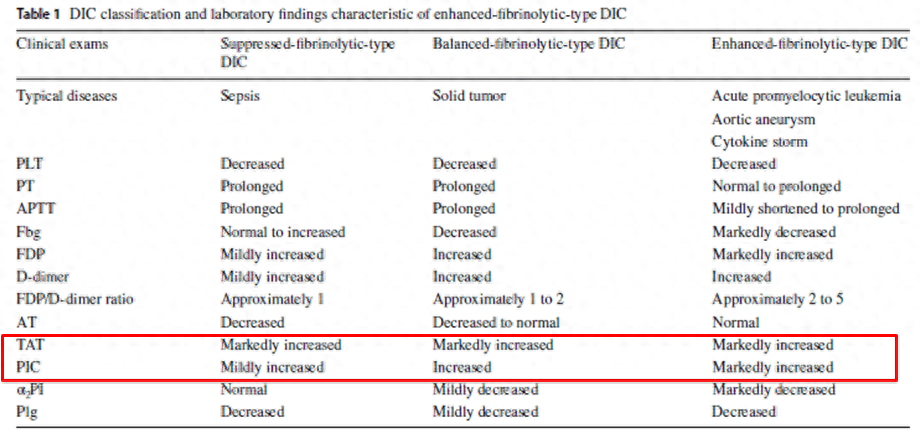
我们进一步检测患者凝血特异标志物,
TAT:59.6ng/mL(Ref<4.0)
PIC: 12.8 ug/mL(Ref<0.8)
两者均显著升高,可首先排除纤溶抑制型DIC。再结合本例的纤维蛋白原水平正常,可排除纤溶增强型DIC,因此本例考虑为
纤溶均衡型DIC
,典型病因即为实体肿瘤。
上述两方面的分析均聚焦肿瘤DIC,因此我们检测本例患者的男性相关肿瘤标志物CEA、AFP、CA199、TPSA,结果患者CEA显著升高达162ng/mL(Ref<5),不排除恶性肿瘤。
随后患者胸部CT平扫考虑右肺原发肿瘤性病变、多发骨转移。确认本例的凝血紊乱为
肿瘤(肺癌骨转移)相关DIC
。
此外,本例的凝血指标不仅有助于病因的排查,也可能有助预后判断:许多与肿瘤相关的凝血因子,包括组织因子、纤维蛋白和纤溶酶,在恶性肿瘤的生长、转移、血栓形成和血管生成过程中失调[1],血浆D-二聚体水平升高反映了这种凝血和纤溶之间的失调。荟萃分析表明多种类型实体肿瘤患者治疗前血浆D-二聚体升高与不良生存率相关[2],也有研究建议将D-二聚体整合进一些肿瘤分期系统。下图为D-二聚体升高与肺癌总体生存率(OS)、无复发生存率(PFS)的相关性汇总[3]:
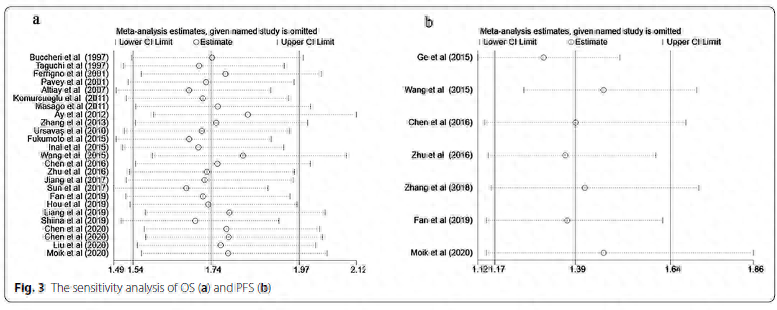
因此,凝血指标不仅有助肿瘤相关DIC的快速判断,也可能有助于评估实体肿瘤患者的转移、分期和预后,值得临床、实验室关注和合理应用。
参考文献
1. Sakurai M, Satoh T, Matsumoto K, et al.: High pretreatment plasma d-dimer levels are associated with poor prognosis in patients with ovarian cancer independently of venous thromboembolism and tumor extension. Int J Gynecol Cancer. 2015, 25:593-8.
2. Li W, Tang Y, Song Y, Chen SH, Sisliyan N, Ni M, Zhang H, Zeng Q, Hou B, Xie X, Chang D. Prognostic Role of Pretreatment Plasma D-Dimer in Patients with Solid Tumors: a Systematic Review and Meta-Analysis. Cell Physiol Biochem. 2018;45(4):1663-1676.
3.Ma M, Cao R, Wang W, Wang B, Yang Y, Huang Y, Zhao G, Ye L. The D-dimer level predicts the prognosis in patients with lung cancer: a systematic review and meta-analysis. J Cardiothorac Surg. 2021 Aug 28;16(1):243.
声明:
本平台旨在为医疗卫生专业人士传递更多医学信息。
本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。
如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。
本平台对发布的内容,并不代表同意其描述和观点。
若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。